Filtrar
214 Questões de concurso encontradas
Página 1 de 43
Questões por página:
Questões por página:
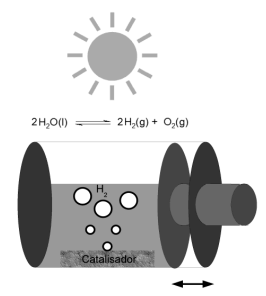
Recentemente, a produção fotocatalítica de hidrogênio vem atraindo atenção devido ao processo que gera um combustível limpo, o qual é utilizado em células a combustível. O processo se baseia na separação da água nos seus componentes, conforme equilíbrio inserido no esquema, utilizando luz solar e um fotocatalisador (p. ex. NaTaO3:La). O processo é extremamente endotérmico, necessitando 1,23 eV para ocorrer. Num experimento, o processo foi realizado num sistema fechado, como esquematizado ao lado. Considerando essas informações, identifique as afirmativas a seguir como verdadeiras (V) ou falsas (F):
( ) A quantidade de fotocatalisador limita a conversão. ( ) O aumento da temperatura irá favorecer a conversão. ( ) A diminuição do volume do sistema irá favorecer a conversão. ( ) É condição necessária para a produção de hidrogênio que o fotocatalisador absorva energia solar superior a 1,23 eV.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
( ) A quantidade de fotocatalisador limita a conversão. ( ) O aumento da temperatura irá favorecer a conversão. ( ) A diminuição do volume do sistema irá favorecer a conversão. ( ) É condição necessária para a produção de hidrogênio que o fotocatalisador absorva energia solar superior a 1,23 eV.

Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
A biodegradação da matéria orgânica produz substâncias húmicas, nas quais os principais componentes são os ácidos húmicos. Estes correspondem a diversas estruturas complexas, que possuem na maioria substituintes fenólicos (pKa = 8) e carboxílicos (pKa = 4). Além de alterar o pH do meio, também são capazes de se ligar a íons metálicos formando coloides. Sobre esse tema, considere as seguintes afirmativas:
1. A presença de substâncias húmicas torna o pH menor que 7. 2. A presença de substâncias húmicas ligadas a íons metálicos é detectada pelo turvamento do meio. 3. O valor medido de pH 6 em uma amostra indica que praticamente todos os substituintes fenólicos estão protonados, enquanto que os substituintes carboxílicos estão desprotonados. 4. O valor medido de pH 4 em uma amostra indica que 50% dos substituintes carboxílicos estão protonados.
Assinale a alternativa correta.
1. A presença de substâncias húmicas torna o pH menor que 7. 2. A presença de substâncias húmicas ligadas a íons metálicos é detectada pelo turvamento do meio. 3. O valor medido de pH 6 em uma amostra indica que praticamente todos os substituintes fenólicos estão protonados, enquanto que os substituintes carboxílicos estão desprotonados. 4. O valor medido de pH 4 em uma amostra indica que 50% dos substituintes carboxílicos estão protonados.
Assinale a alternativa correta.
mostrar texto associado
Ainda no contexto do acidente anteriormente mencionado, considere que 1,0 × 105 mol de H2SO4 tenham atingido um lago com volume de água igual a 1,0 × 109 L e que esse ácido tenha se distribuído rapidamente por toda extensão do lago, formando uma solução homogênea. Considere, também, que, antes da contaminação, a água do lago fosse neutra, que a autoprotólise da água seja uma reação altamente endotérmica e que, a 25 ºC, o valor de sua constante seja igual a 1,0 × 10–14 . Com base nessas informações e desprezando os desvios de idealidade e a ocorrência de reações paralelas às de ionização do ácido e de autoprotólise da água, julgue os itens a seguir.
Considerando-se que a primeira ionização do H2SO4 seja praticamente completa e a segunda, parcial, é correto concluir que o pH da água do lago, após a contaminação pelo ácido, atinge valor inferior a 4,0.
Considerando-se que a primeira ionização do H2SO4 seja praticamente completa e a segunda, parcial, é correto concluir que o pH da água do lago, após a contaminação pelo ácido, atinge valor inferior a 4,0.
mostrar texto associado
Ainda no contexto do acidente anteriormente mencionado, considere que 1,0 × 105 mol de H2SO4 tenham atingido um lago com volume de água igual a 1,0 × 109 L e que esse ácido tenha se distribuído rapidamente por toda extensão do lago, formando uma solução homogênea. Considere, também, que, antes da contaminação, a água do lago fosse neutra, que a autoprotólise da água seja uma reação altamente endotérmica e que, a 25 ºC, o valor de sua constante seja igual a 1,0 × 10–14 . Com base nessas informações e desprezando os desvios de idealidade e a ocorrência de reações paralelas às de ionização do ácido e de autoprotólise da água, julgue os itens a seguir.
Caso o acidente em questão tenha ocorrido em um dia frio, com a temperatura da água a 5 ºC, é correto concluir que, no instante imediatamente anterior ao derramamento, o pH da água do lago era superior a 7,0.
Caso o acidente em questão tenha ocorrido em um dia frio, com a temperatura da água a 5 ºC, é correto concluir que, no instante imediatamente anterior ao derramamento, o pH da água do lago era superior a 7,0.
Em um laboratório, um técnico precisou identificar soluções 0,1 mol/L de CH3COOH, NaOH e NaCℓ contidas em três frascos cujos rótulos foram danificados. Para isso, ele numerou os frascos e adicionou fenolftaleína e metilorange, separadamente, a cada um deles, observando os seguintes resultados:
Solução do frasco I: ficou rosa em fenolftaleína e amarela no metilorange.
Solução do frasco II: permaneceu incolor em fenolftaleína e vermelha no metilorange.
Solução do frasco III: permaneceu incolor em fenolftaleína e amarela no metilorange.
Sabe-se que a fenolftaleína, em pH acima de 9 apresenta coloração vermelha, enquanto que, em pH abaixo desse valor, é incolor. Sabe-se ainda que o metilorange apresenta coloração vermelha em pH abaixo de 3,5 e amarela em pH acima deste valor.
Sendo assim, os estudantes chegaram à conclusão de que os frascos I, II e III contêm, respectivamente, solução de
Solução do frasco I: ficou rosa em fenolftaleína e amarela no metilorange.
Solução do frasco II: permaneceu incolor em fenolftaleína e vermelha no metilorange.
Solução do frasco III: permaneceu incolor em fenolftaleína e amarela no metilorange.
Sabe-se que a fenolftaleína, em pH acima de 9 apresenta coloração vermelha, enquanto que, em pH abaixo desse valor, é incolor. Sabe-se ainda que o metilorange apresenta coloração vermelha em pH abaixo de 3,5 e amarela em pH acima deste valor.
Sendo assim, os estudantes chegaram à conclusão de que os frascos I, II e III contêm, respectivamente, solução de
