Questões de Concurso
Filtrar
107 Questões de concurso encontradas
Página 10 de 22
Questões por página:
Em condições ideais, pequenas quantidades de gás cloro podem ser geradas em laboratório pela reação do óxido de manganês (MnO2 ) com ácido clorídrico (HCl), conforme a equação química a seguir não balanceada.
HCl(aq) + MnO2 (s) → H2O(L) + MnCl2(s) + Cl2(g)
A partir dessas informações, quantas moléculas de gás cloro, aproximadamente, podem ser produzidas quando 10 g de óxido de manganês com grau de pureza de 87% são colocados para reagir completamente com excesso de ácido clorídrico?
Dado: Número de Avogadro (N) = 6 x 1023
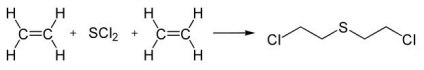
Sobre a equação de produção do gás mostarda, foram feitas a seguintes afirmações:
I. O eteno é um composto isomérico trans. II. O gás mostarda tem fórmula molecular C4H8SCl2 . III. A reação orgânica de produção do gás mostarda é de substituição.
São incorretas as afirmações
Butano é o gás armazenado em botijões ou encanamentos, usado no cozimento dos alimentos.
O gás butano, derivado do petróleo, é uma substância inodora e incolor. Devido a essas características outros elementos costumam ser acrescentados ao butano, para que, em caso de vazamento, possa se sentir o cheiro e evitar possíveis acidentes.

A combustão completa desse gás produz gás carbônico e água segundo a equação não balanceada a seguir
C4H10(g) + O2(g) → CO2(g) + H2O(l)
O balanceamento correto dessa equação permite concluir que, para cada molécula de butano queimada, há produção de
CrCl3 + NaOH + H2O2 → Na2CrO4 + NaCl + H2O
