Filtrar
281 Questões de concurso encontradas
Página 1 de 57
Questões por página:
Questões por página:
Em uma reação química classificada como exotérmica, é correto afirmar que os produtos:
mostrar texto associado
Ainda considerando-se as informações do texto anterior, é correto afirmar que a hidrólise da sacarose, produzindo glicose e frutose, é uma reação
A análise dos dados termodinâmicos de reações permite a previsão da espontaneidade. Na tabela a seguir estão apresentados os dados termodinâmicos de duas reações químicas.
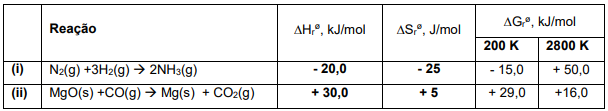
A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i). ( ) O aumento da temperatura favorece a espontaneidade da reação (ii). ( ) Na temperatura de 400 K, a reação (i) será espontânea. ( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.

A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i). ( ) O aumento da temperatura favorece a espontaneidade da reação (ii). ( ) Na temperatura de 400 K, a reação (i) será espontânea. ( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Águas termais, exploradas em diversos destinos turísticos, brotam naturalmente em fendas rochosas. O aquecimento natural dessas águas, na sua grande maioria, deve-se ao calor liberado em processos radioativos de elementos presentes nos minerais rochosos que são transferidos para a água no fluxo pelas fendas. O gás radônio (222Rn) é o provável responsável pelo aquecimento de diversas águas termais no Brasil. O 222Rn se origina do rádio (226Ra), na série do urânio (238U), naturalmente presente em granitos. O tempo de meia vida (t1/2) do 222Rn é de 3,8 dias, e esse se converte em polônio (218Po), que por sua vez possui um t1/2 de 3,1 minutos. Considerando as informações dadas, considere as seguintes afirmativas:
1. A conversão de 222Rn em 218Po é um processo exotérmico. 2. A conversão de226Ra em 222Rn emite quatro partículas . 3. Na série de decaimento, do 238U ao 218Po, cinco partículas
. 3. Na série de decaimento, do 238U ao 218Po, cinco partículas  são emitidas.4. Após 3,8 dias da extração da água termal, a concentração de 218Po atingirá a metade do valor da concentração inicial de 222Rn.
são emitidas.4. Após 3,8 dias da extração da água termal, a concentração de 218Po atingirá a metade do valor da concentração inicial de 222Rn.
Assinale a alternativa correta.
1. A conversão de 222Rn em 218Po é um processo exotérmico. 2. A conversão de226Ra em 222Rn emite quatro partículas
 . 3. Na série de decaimento, do 238U ao 218Po, cinco partículas
. 3. Na série de decaimento, do 238U ao 218Po, cinco partículas  são emitidas.4. Após 3,8 dias da extração da água termal, a concentração de 218Po atingirá a metade do valor da concentração inicial de 222Rn.
são emitidas.4. Após 3,8 dias da extração da água termal, a concentração de 218Po atingirá a metade do valor da concentração inicial de 222Rn. Assinale a alternativa correta.
