Questões de Concurso
Filtrar
337 Questões de concurso encontradas
Página 47 de 68
Questões por página:
Podemos observar no trecho que há incoerência relacionada à experiência de Rutherford e seus colaboradores.
Assinale a alternativa que refere-se ao ERRO encontrado no trecho.
I. Calcule o trabalho quando o gás passa de A para C, através de um processo de um estágio. II. Idem em 2 estágios, passando pelo ponto B. III. Idem em infinitos estágios. IV. Calcule o trabalho quando o gás passa de C para A, através de um processo de um estágio. V. Idem em infinitos estágios.
 Dados: 1 pascal (1 Pa) = 1 N/m² 1 atmosfera (atm) = 1,013×105 N/m2 = 101,3 kPa 1 atm = 760 mmHg 1 torr = 1 mmHg = 133,3 Pa 1 atm.l = 101,3 J
Dados: 1 pascal (1 Pa) = 1 N/m² 1 atmosfera (atm) = 1,013×105 N/m2 = 101,3 kPa 1 atm = 760 mmHg 1 torr = 1 mmHg = 133,3 Pa 1 atm.l = 101,3 J A resposta correta para o conjunto de questões de I a V, respectivamente, é:
 Identifique as transformações representadas por A→B, B→C, C→D, D→A e A→C e assinale a alternativa correta:
Identifique as transformações representadas por A→B, B→C, C→D, D→A e A→C e assinale a alternativa correta: Após analisar as afirmativas de I a V, assinale a alternativa correta:
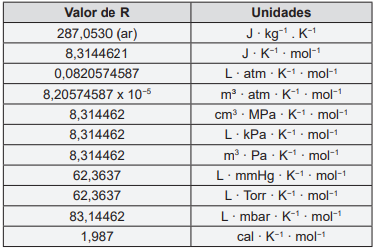
Considere a tabela abaixo para responder a questão 60:
Analise as afirmativas abaixo e assinale a alternativa em que a obtenção do ferro a partir da hematita pode ser descrita pela equação: Fe2O3 + 3CO → 2Fe + 3CO2 .
I. A massa de ferro que será obtida a partir de 0,04 mol de óxido férrico é 4,48 g.
II. A quantidade de CO necessários para produzir 7 mol de ferro é 10,5 mol.
III. A massa de gás carbônico obtida partindo-se de 20 kg de óxido de ferro III será 16,5 g.
IV. A quantidade de monóxido de carbono necessária para reagir com 600 g de óxido férrico é 11,25 mol.
V. O volume de CO, medidos nas CNTP, consumido na obtenção de 60 kg de ferro será ~3,6 104 L.
Após analisar as afirmativas de I a V, assinale a alternativa correta: