Filtrar
72 Questões de concurso encontradas
Página 1 de 15
Questões por página:
Questões por página:
Concurso:
IF Farroupilha - RS
Disciplina:
Química
A cinética química estuda os fatores que influenciam a velocidade das reações químicas e os mecanismos pelos quais elas ocorrem. Considerando os conceitos fundamentais da cinética química, analise as assertivas abaixo:
I. A energia de ativação de uma reação química pode ser reduzida pelo aumento da temperatura do sistema.
II. Reações que ocorrem em uma única etapa (elementares) apresentam velocidades independentes da concentração dos reagentes.
III. A velocidade de uma reação química pode ser influenciada por diversos fatores, tais como: temperatura, uso de catalisador e concentração de reagentes.
Quais estão corretas?
I. A energia de ativação de uma reação química pode ser reduzida pelo aumento da temperatura do sistema.
II. Reações que ocorrem em uma única etapa (elementares) apresentam velocidades independentes da concentração dos reagentes.
III. A velocidade de uma reação química pode ser influenciada por diversos fatores, tais como: temperatura, uso de catalisador e concentração de reagentes.
Quais estão corretas?
Dada a reação hipotética:

A partir de dados experimentais, verifica-se que o composto A é um reagente de terceira ordem e a substância B é um reagente de primeira ordem da reação.
Se duplicarmos as concentrações dos reagentes A e B, a velocidade dessa reação aumentará:
Um composto M foi produzido a partir da reação entre 8,4 g de propeno e 4,0 g de água, em meio ácido e à temperatura de 170 0 C. Metade da massa do composto M produzido é colocado para reagir com solução aquosa de permanganato de potássio em meio ácido produzindo um composto T, com um rendimento de 50%. A massa, em gramas, do composto T produzido é:
No estudo da cinética química, frequentemente mecanismos de reação propostos precisam ser verificados contra dados experimentais. Nessa abordagem, antes de determinar a lei de velocidade total, é conveniente descrever as reações elementares de cada etapa do mecanismo proposto. Suponha a seguinte reação elementar fictícia:
A + A -> C + D
A molecularidade dessa reação é:
A + A -> C + D
A molecularidade dessa reação é:
A Termoquímica é o ramo da Química que estuda o calor absorvido ou liberado em uma transformação física ou química (reação), pois cada substância armazena uma determinada quantidade de calor, que será alterado quando a substância sofrer alguma transformação. Observe o gráfico a seguir que representa o caminho da reação genérica balanceada.
A2 + B2 → 2 AB
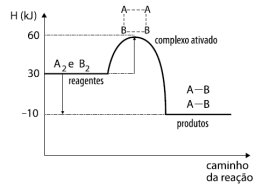
Disponível em: i_662d64349cafcb5b_html_55011cd1.png (463×350) (quimicaevestibular.com.br). Acesso em 27 de Julho de 2021.
Com relação ao gráfico acima, temos as seguintes afirmativas: I. A reação absorve calor; II. A energia de ativação da reação é 60 KJ; III. O valor da entalpia da reação (∆H) é de -40 KJ; IV. Ao colocarmos um catalisador na reação, diminuímos a sua entalpia (∆H), tornando-a mais rápida.
Estão corretas as afirmativas:
A2 + B2 → 2 AB

Disponível em: i_662d64349cafcb5b_html_55011cd1.png (463×350) (quimicaevestibular.com.br). Acesso em 27 de Julho de 2021.
Com relação ao gráfico acima, temos as seguintes afirmativas: I. A reação absorve calor; II. A energia de ativação da reação é 60 KJ; III. O valor da entalpia da reação (∆H) é de -40 KJ; IV. Ao colocarmos um catalisador na reação, diminuímos a sua entalpia (∆H), tornando-a mais rápida.
Estão corretas as afirmativas: