Questões de Concurso
Filtrar
202 Questões de concurso encontradas
Página 21 de 41
Questões por página:
Questões por página:
Nos últimos meses, tem-se discutido sobre o uso de uma substância química, a fosfoetanolamina, anunciada como a cura para diversos tipos de cânceres. A estrutura química da fosfoetalonamina é descrita a seguir e tem o fósforo como o átomo central.
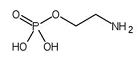
Sobre a estrutura química da fosfoetalonamina, analise as seguintes afirmativas:
I. A geometria molecular da fosfoetanolamina é piramidal.
II. A fosfoetalonamina tem 15 ligações sigma e uma pi.
III. A fosfoetalonamina é um composto covalente polar.
Estão CORRETAS as afirmativas:
A figura seguinte representa um experimento de eletrólise da água.
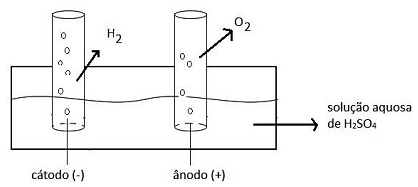
Com relação ao experimento, dentre as substâncias iniciais e as que foram formadas no processo de eletrólise da água, são consideradas substância simples, composta e mistura, respectivamente:

Com relação ao experimento, dentre as substâncias iniciais e as que foram formadas no processo de eletrólise da água, são consideradas substância simples, composta e mistura, respectivamente:
A intensidade das forças intermoleculares em diferentes substâncias varia em uma grande faixa, mas essas forças são muito mais fracas que as ligações iônicas e covalentes. Dessa forma, é necessário menos energia para vaporizar um líquido ou fundir um sólido do que quebrar ligações covalentes em moléculas.
Ponto de ebulição dos hidretos do grupo 4A e 6A em função da massa molecular.
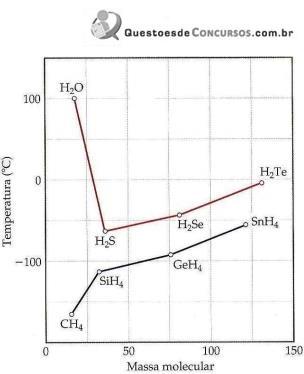
(Química Ciência Central.)
Sobre a imagem e intensidade das forças intermoleculares, analise.
I. No geral, o ponto de ebulição de compostos de hidrogênio torna-se maior com o aumento da massa molecular, devido ao acréscimo das forças de dispersão.
II. Os compostos NH3 e HF também têm pontos de ebulição altos.
III. A ligação de hidrogênio é um tipo de atração intermolecular entre o átomo de hidrogênio em uma ligação apolar (particularmente uma ligação com F, O ou N) e um par de elétrons não compartilhado em um íon ou átomo pequeno e eletronegativo que esteja próximo (geralmente um átomo de F, O ou N em outra molécula).
Está(ão) correta(s) apenas a(s) afirmativa(s)
Ponto de ebulição dos hidretos do grupo 4A e 6A em função da massa molecular.

(Química Ciência Central.)
Sobre a imagem e intensidade das forças intermoleculares, analise.
I. No geral, o ponto de ebulição de compostos de hidrogênio torna-se maior com o aumento da massa molecular, devido ao acréscimo das forças de dispersão.
II. Os compostos NH3 e HF também têm pontos de ebulição altos.
III. A ligação de hidrogênio é um tipo de atração intermolecular entre o átomo de hidrogênio em uma ligação apolar (particularmente uma ligação com F, O ou N) e um par de elétrons não compartilhado em um íon ou átomo pequeno e eletronegativo que esteja próximo (geralmente um átomo de F, O ou N em outra molécula).
Está(ão) correta(s) apenas a(s) afirmativa(s)
Considere as substâncias H2O, CH4 e H2S.
A ordem crescente de ponto de ebulição para essas substâncias é
A ordem crescente de ponto de ebulição para essas substâncias é
Para separar líquidos de sólidos no processo de tratamento de água e efluentes, podem ser utilizadas microbolhas de ar que arrastam impurezas em suspensão para a superfície, facilitando sua remoção. Nesse processo, as microbolhas se prendem às partículas sólidas e óleos, formando aglomerados que, carregados para a superfície, formam uma espuma que, então, é retirada.
O processo de separação descrito acima denomina-se
O processo de separação descrito acima denomina-se