Questões de Concurso
Filtrar
71 Questões de concurso encontradas
Página 9 de 15
Questões por página:
Questões por página:
A reação em fase gasosa a A + b B → c C + d D foi estudada em diferentes condições de concentração inicial dos reagentes, tendo sido obtidos os seguintes resultados experimentais, todos na mesma temperatura:

A partir dos dados experimentais da tabela, indique a alternativa que apresenta o valor correto da velocidade inicial da reação no experimento IV.
Para que uma reação química possa ocorrer é necessário que os reagentes recebam certa quantidade de energia, chamada energia de ativação (Ea). A reação entre os gases nitrogênio e oxigênio, componentes do ar, por exemplo, não ocorre em condições ambientes, embora exista um grande número de choques entre suas moléculas. A reação entre esses gases ocorre na atmosfera apenas quando associada a descargas elétricas dos relâmpagos, em dias chuvosos, e também no interior dos motores de explosões internas, quando a vela do automóvel libera uma faísca elétrica. Nesses casos, a Ea é fornecida pelas faíscas.
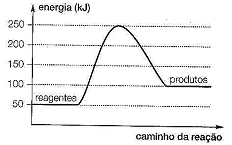
Considerando o gráfico anterior, referente ao diagrama energético de uma reação química, qual o valor da energia de ativação e o ΔH da reação respectivamente?

Considerando o gráfico anterior, referente ao diagrama energético de uma reação química, qual o valor da energia de ativação e o ΔH da reação respectivamente?
Questão Anulada
A expressão de velocidade para a reação descrita a seguir, é corretamente apresentada na alternativa.

mostrar texto associado
Em função dos dados fornecidos, pode-se afirmar que o tipo de substituição nucleofílica e a lei de velocidade da reação são, respectivamente:
Diariamente, inúmeras situações mostram a influência da temperatura na rapidez com que as reações químicas se processam. Por exemplo, a efervescência de um comprimido antiácido é maior em água à temperatura ambiente do que em água gelada. Os alimentos são colocados na geladeira, pois uma diminuição da temperatura faz com que a decomposição dos alimentos por micro-organismos ocorra de forma mais lenta. Em um experimento, a constante de velocidade (k) para a decomposição de primeira ordem de um composto em solução foi determinada a várias temperaturas (T), conforme mostra a tabela a seguir: K 0,00492 0,0216 0,095 0,330 1,15 T (K) 278 288 298 308 318
A energia de ativação para a reação de decomposição pode ser calculada a partir da tabela e seu valor, em kJ.mol -1 , é aproximadamente igual a:
Dados: R= 8,31 J.mol -1. k-1 , ln 4,4 = 1,48; ln 3,5 = 1,25
A energia de ativação para a reação de decomposição pode ser calculada a partir da tabela e seu valor, em kJ.mol -1 , é aproximadamente igual a:
Dados: R= 8,31 J.mol -1. k-1 , ln 4,4 = 1,48; ln 3,5 = 1,25