Concurso:
MPU
Disciplina:
Engenharia Química
mostrar texto associado
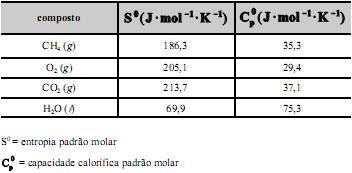
Considerando-se que as capacidades caloríficas fornecidas na tabela sejam válidas para o intervalo de temperaturas entre 25 ºC e 35 ºC, é correto afirmar que a combustão do CH4 (g) deverá liberar maior quantidade de calor se for realizada a 35 ºC, e não a 25 ºC.