Questões de Concurso
Filtrar
2.583 Questões de concurso encontradas
Página 218 de 517
Questões por página:
Questões por página:
Um elemento pertencente ao grupo dos halogênios é:
Considerando as reações a seguir:
 .
.
 ,
,
OΔH da reação a seguir é igual a:
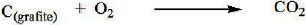 .
.
mostrar texto associado
Está correto somente o que se afirma em:
Uma reação de dupla troca é apresentada na alternativa:
Afórmula química do ácido clórico é: