Questões de Concurso
Filtrar
2.558 Questões de concurso encontradas
Página 289 de 512
Questões por página:
Questões por página:
No passado, as cargas das baterias dos celulares chegavam a durar até uma semana, no entanto, atualmente, o tempo entre uma recarga e outra dificilmente ultrapassa 24 horas. Isso não se deve à má qualidade das baterias, mas ao avanço tecnológico na área de baterias, que não acompanha o aumento das funcionalidades dos smartphones. Atualmente, as baterias recarregáveis são do tipo íon-lítio, cujo esquema de funcionamento está ilustrado na figura ao lado.
Quando a bateria está em uso (atuando como uma pilha), o anodo corresponde ao componente:

Quando a bateria está em uso (atuando como uma pilha), o anodo corresponde ao componente:

Adicionar sal de cozinha ao gelo é uma prática comum quando se quer “gelar" bebidas dentro da geleira. A adição do sal faz com que a temperatura de fusão se torne inferior à da água pura.
(Dados: Kf = 1,86 ºC.kg.mol-1 ; M(g.mol-1 ): Cl = 35,5; Na = 23)
A diferença na temperatura de fusão (em °C) na mistura obtida ao se dissolver 200 g de sal de cozinha em 1 kg de água, em relação à água pura, é de:
(Dados: Kf = 1,86 ºC.kg.mol-1 ; M(g.mol-1 ): Cl = 35,5; Na = 23)
A diferença na temperatura de fusão (em °C) na mistura obtida ao se dissolver 200 g de sal de cozinha em 1 kg de água, em relação à água pura, é de:
A extração de petróleo em águas profundas segue basicamente três etapas: i) perfuração, utilizando uma sonda; ii) injeção de água pressurizada, que extrai o petróleo das rochas subterrâneas; e iii) separação do petróleo misturado com água e pedaços de rochas.
A terceira etapa é realizada por meio dos métodos de:
A terceira etapa é realizada por meio dos métodos de:
Os medidores de glicose digitais são dispositivos bastante difundidos e essenciais para pessoas que têm diabetes. Esses dispositivos são baseados em sensores de glicose, cujo teor é medido por meio de uma reação química. Uma proposta se baseia na seguinte reação:

Nesse sistema de medição, faz-se reagir uma amostra contendo glicose com o íon ferricianeto ([Fe(CN)6]3- ) na presença da enzima GOx, obtendo-se como produtos gluconolactona, H+ e ferrocianeto ([Fe(CN)6]4- ). Um eletrodo de platina promove a reação de regeneração do ferricianeto, sendo que a corrente que passa por esse eletrodo é proporcional à concentração de glicose na amostra.
Com base no exposto, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) A enzima GOx catalisa a oxidação da glicose.
( ) No eletrodo de platina ocorre a redução do íon de ferro.
( ) A transformação de glicose em gluconolactona envolve 2 elétrons.
( ) O valor de pH do meio tende a diminuir no processo de detecção de glicose.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.

Nesse sistema de medição, faz-se reagir uma amostra contendo glicose com o íon ferricianeto ([Fe(CN)6]3- ) na presença da enzima GOx, obtendo-se como produtos gluconolactona, H+ e ferrocianeto ([Fe(CN)6]4- ). Um eletrodo de platina promove a reação de regeneração do ferricianeto, sendo que a corrente que passa por esse eletrodo é proporcional à concentração de glicose na amostra.
Com base no exposto, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) A enzima GOx catalisa a oxidação da glicose.
( ) No eletrodo de platina ocorre a redução do íon de ferro.
( ) A transformação de glicose em gluconolactona envolve 2 elétrons.
( ) O valor de pH do meio tende a diminuir no processo de detecção de glicose.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
A análise dos dados termodinâmicos de reações permite a previsão da espontaneidade. Na tabela a seguir estão apresentados os dados termodinâmicos de duas reações químicas.
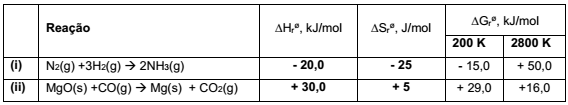
A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i).
( ) O aumento da temperatura favorece a espontaneidade da reação (ii).
( ) Na temperatura de 400 K, a reação (i) será espontânea.
( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.