Questões de Concurso
Filtrar
2.002 Questões de concurso encontradas
Página 290 de 401
Questões por página:
Questões por página:
Concurso:
TRANSPETRO
Disciplina:
Química
A teoria para o cálculo da força de empuxo está diretamente relacionada ao Princípio de Archimedes que diz: todo corpo imerso em um fluido em equilíbrio, dentro de um campo gravitacional, é sujeito a uma força vertical aplicada pelo fluido, com sentido
Concurso:
TRANSPETRO
Disciplina:
Química

A figura mostra um manômetro diferencial, onde o fluido A é salmoura, B é óleo, e o fluido manométrico é mercúrio. Sendo h1 = 40 cm, h2 = 120 cm, h3 = 90 cm e h4 = 15 cm, qual é a diferença de pressão entre os pontos A e B, expressa em kPa?
Dados:
Massa específica da salmoura ρsalmoura = 1200 kg/m³
Massa específica do mercúrio ρHg = 13600 kg/m³
Massa específica do óleo ρóleo = 800 kg/m³
Aceleração da gravidade g = 10 m/s2
Concurso:
TRANSPETRO
Disciplina:
Química
Um gás ideal a 27 °C se expande reversivel e isotermicamente de 20 L a 60 L em um sistema que contém 2 mols desse gás em sua composição.
O trabalho, em joules, trocado com o ambiente durante tal processo de expansão, é
Dados:
Constante universal dos gases R= 8,31 J.K−1.mol−1
1 L.atm = 101,3 J
ln 3 = 1,1
Concurso:
TRANSPETRO
Disciplina:
Química
A figura ilustra a eletrodeposição, processo inverso ao da pilha. É um dos mais importantes métodos de revestimento aplicados a materiais para protegê-los da corrosão.
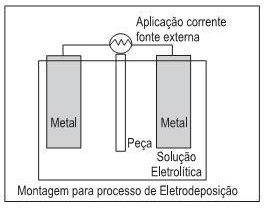
Esse processo consiste na aplicação de células eletrolíticas que utilizam energia elétrica para produzir reações de oxirredução não espontâneas, além de permitir o(a)
Concurso:
TRANSPETRO
Disciplina:
Redes de Computadores
Um recipiente, cuja capacidade é de 20 L, contém uma mistura gasosa ideal de 2,0 g de cada um dos seguintes gases: N 2, H2 e O2 .
Se a temperatura da mistura é de 27 °C, a pressão, em atm, é, aproximadamente, de
Se a temperatura da mistura é de 27 °C, a pressão, em atm, é, aproximadamente, de
Dados:
Constante universal dos gases R = 0,082 L.atm.K−1 .mol−1
Peso atômico do hidrogênio = 1
Peso atômico do oxigênio = 16
Peso atômico do nitrogênio = 14