70 Questões de concurso encontradas
Página 8 de 14
Questões por página:
A entalpia específica h(p,T) e a energia livre de Gibbs específica g definida por: g = h – Ts são funções de estado e, portanto, as suas expressões na forma diferencial, dh e dg, respectivamente, são diferenciais exatas. A partir da definição de entalpia e da forma diferencial da equação de conservação de energia para um sistema fechado, contendo um fluido compressível, obtém-se a expressão:
dh = Tds + vdp.
Usando uma das relações de Maxwell, a variação da entalpia com relação à pressão, mantendo-se a temperatura constante, 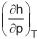 é determinada pela expressão
é determinada pela expressão
As propriedades termodinâmicas dos fluidos: energia interna, entalpia e entropia específicas podem ser calculadas a partir das propriedades temperatura, pressão e volume específico, que são mensuráveis. Se for escolhida adequadamente a dependência dessas propriedades, relações importantes podem ser obtidas.
Definindo-se a dependência: h = h(s,p), a seguinte expressão é obtida:
Uma determinada massa de gás ideal, inicialmente a uma pressão e temperatura  , é submetida a um processo de alteração de suas variáveis de estado até que estas atinjam novos valores
, é submetida a um processo de alteração de suas variáveis de estado até que estas atinjam novos valores 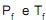 . Esse processo é baseado em duas etapas em sequência:
. Esse processo é baseado em duas etapas em sequência:
1ª – Aquecimento à pressão constante até atingir a temperatura 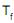 .
.
2ª – Compressão isotérmica do gás até atingir uma pressão  .
.
Considerando-se que a capacidade calorífica à pressão constante 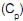 mantém o mesmo valor ao longo do processo, a variação da energia interna do sistema é igual a
mantém o mesmo valor ao longo do processo, a variação da energia interna do sistema é igual a

